L'Agence européenne des médicaments lance l'examen d'une pilule anti-Covid
- Avec AFP
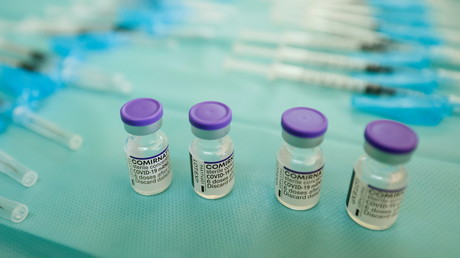
 © Handout / Merck & Co,Inc. Source: AFP
© Handout / Merck & Co,Inc. Source: AFPL'Agence Européenne des médicaments va examiner une pilule anti-Covid développée par le laboratoire américain Merck, qui a demandé une autorisation d'urgence aux Etats-Unis. Cette pilule ne pourra cependant pas se substituer à la vaccination.
L'Agence européenne des médicaments (AEM) a annoncé le 25 octobre le lancement de l'examen accéléré de la pilule contre le Covid-19 du laboratoire étasunien Merck, un remède facile à administrer et appelé à devenir un outil crucial dans la lutte contre la pandémie, car complémentaire des vaccins.
Cette étape, ouvrant la voie à une éventuelle prochaine demande d'autorisation dans l'Union européenne du traitement pris par comprimés, survient deux semaines après que Merck a demandé en urgence aux Etats-Unis une autorisation pour ce médicament.
«Le comité des médicaments à usage humain [CHMP] de l'AEM a lancé un examen continu du médicament antiviral oral molnupiravir [...] développé par Merck [...] pour le traitement du Covid-19 chez les adultes», a déclaré dans un communiqué le régulateur européen installé à Amsterdam.
Les antiviraux comme le molnupiravir agissent en diminuant la capacité d'un virus à se répliquer, freinant ainsi la maladie selon son développeur. Donné à des patients dans les quelques jours suivant un test positif, le traitement réduit par deux les risques d'hospitalisation, selon un essai clinique mené par Merck.
Les résultats préliminaires d'études de laboratoire et d'études cliniques «suggèrent que le médicament peut réduire la capacité du SARS-CoV-2 [...] à se multiplier dans le corps, empêchant ainsi l'hospitalisation ou le décès chez les patients atteints du Covid-19», a précisé l'AEM.
La pilule ne pourra pas se substituer à la vaccination, prévient le laboratoire Merck
L'AEM évaluera la conformité du Molnupiravir aux normes européennes habituelles en matière d'efficacité, de sécurité et de qualité. Un examen continu est un outil réglementaire que le régulateur européen utilise pour accélérer l'évaluation d'un médicament ou d'un vaccin prometteur lors d'une urgence de santé publique. S'il est approuvé, le Molnupiravir représenterait ainsi une avancée en permettant de réduire assez facilement les formes graves de la maladie. Ce type de traitement pour traiter le coronavirus, qui peut être pris chez soi avec un verre d'eau, est recherché depuis le début de la pandémie.
L'annonce de Merck aux Etats-Unis il y a deux semaines avait été saluée comme une étape majeure vers cet objectif mais les experts ont averti que ce traitement ne constituait pas un remède miracle et qu'il devrait compléter les vaccins, pas les remplacer. Merck est également en train de mener un essai clinique distinct pour une seconde utilisation du traitement, à titre préventif pour les personnes ayant été en contact rapproché avec le virus pour ne pas le développer.